JSI-1187的I期臨床試驗(yàn)是一項(xiàng)開放標(biāo)簽、多中心劑量遞增和擴(kuò)展臨床研究��,在攜帶MAPK突變的復(fù)發(fā)����、難治性實(shí)體腫瘤患者中評估JSI-1187的安全性、耐受性����、藥代動力學(xué)����、藥理動力學(xué)和臨床藥效����。該臨床研究包括3個階段:1)JSI-1187單藥劑量爬坡階段,用于實(shí)體腫瘤患者���;2)JSI-1187與BRAF抑制劑達(dá)拉非尼聯(lián)用的劑量爬坡��;3)對攜帶特定基因突變腫瘤患者的擴(kuò)展研究�����。
負(fù)責(zé)JSI-1187項(xiàng)目開發(fā)的首席開發(fā)官Linda Paradiso博士表示:“JSI-1187是選擇性ERK1/2激酶抑制劑�����,我們希望通過ERK抑制劑來對抗攜帶MAPK通路突變的腫瘤��,能夠開發(fā)更有效的單藥和聯(lián)合療法��,在耐藥產(chǎn)生早期階段防止和解決目前已有的MAPK通路靶向藥常見的耐藥問題'�����。
捷思英達(dá)首席執(zhí)行官張勁濤博士表示:“JSI-1187臨床試驗(yàn)的啟動對捷思英達(dá)是一個非常重要的里程碑�����。JSI-1187是捷思英達(dá)首個自主創(chuàng)新研發(fā)并進(jìn)入臨床研究的抗癌新藥���,從項(xiàng)目立項(xiàng)到進(jìn)入臨床試驗(yàn),總共耗費(fèi)約三年時間�。在抗擊新冠疫情,確保安全的前提下���,捷思英達(dá)和合作單位共同努力����,先后在美國國家癌癥研究院(NCI)指定的四家綜合性癌癥中心啟動了臨床試驗(yàn)�。我們期待JSI-1187能為腫瘤患者帶來福音?����!?/span>
JSI-1187是由捷思英達(dá)自主開發(fā)的口服高選擇性ERK1/2小分子激酶抑制劑��,在臨床前模型中對MAPK 通路突變的腫瘤顯示出高度抑制性���。通過 RAS-RAF-MEK-ERK 級聯(lián)的 MAPK 信號在癌癥生長和增殖中起著至關(guān)重要的作用�����。MAPK/ERK 通路的突變存在于多種癌癥類型中���,包括胰腺癌(+90%)�����、膽道癌(3-50%)���、結(jié)直腸癌(30-50%)、肺癌(25-30%)��、卵巢癌(15-39%)和子宮內(nèi)膜 (18%)中的KRAS突變�,以及黑色素瘤 的NRAS突變 (20%)和BRAF V600突變(50%)等。雖然BRAF/MEK抑制劑靶向聯(lián)合療法在黑色素瘤和其他癌癥中比單藥具有更顯著的藥效��,但大多數(shù)患者最終都會產(chǎn)生耐藥性和疾病進(jìn)展����。在已發(fā)現(xiàn)的耐藥機(jī)制中,關(guān)鍵是ERK激酶的重新激活。因此��,ERK 抑制具有避免或克服耐藥的潛力�����。
目前全球尚無ERK激酶抑制劑獲批上市�����,進(jìn)展最快的項(xiàng)目也僅處于II期階段����,包括優(yōu)立替尼(BioMed Valley Discoveries/Vertex)���、LY3214996(禮來)��、LTT462(諾華)�。JSI-1187于2020年1月獲得美國FDA臨床申請?jiān)S可�,2020年6月在美國啟動臨床I期試驗(yàn)(臨床試驗(yàn)登記號為:NCT04418167)。
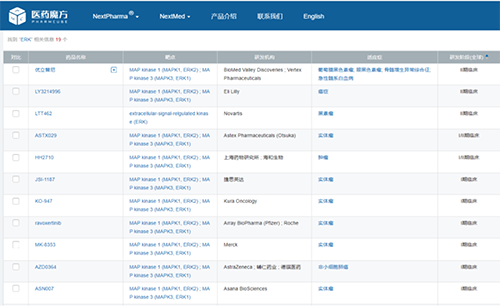
來源:NextPharma
關(guān)于捷思英達(dá)
捷思英達(dá)位于上海張江科學(xué)城國際醫(yī)學(xué)園區(qū)����,專注于小分子原創(chuàng)抗癌新藥的研發(fā)。捷思英達(dá)在上海張江國際醫(yī)學(xué)園區(qū)擁有包括動物房在內(nèi)的新藥探新研究技術(shù)平臺,在美國波士頓設(shè)有負(fù)責(zé)項(xiàng)目引進(jìn)和臨床開發(fā)的子公司�。捷思英達(dá)采用自主研發(fā)和項(xiàng)目引進(jìn)齊頭并進(jìn)的“雙輪驅(qū)動”商業(yè)模式,加快研發(fā)管線的建立���。公司研發(fā)團(tuán)隊(duì)及時應(yīng)用國際知名臨床專家最新發(fā)現(xiàn)的藥物作用機(jī)制����,開展國際首創(chuàng)的抗癌新藥研發(fā)���,努力解決國內(nèi)外腫瘤患者高度未滿足的臨床需求����。